16: Solvatering og overføring mellom faser
Contents
16: Solvatering og overføring mellom faser#
I systemer av to komponenter der én av komponentene kan forlate den kondenserte fasen til gassfase, eller til andre kondenserte faser, avhenger denne partikkelutvekslingen av konsentrasjonen til den komponenten i løsningen. Slike systemer kan studeres gjennom gittermodeller for å forklare, blant annet, hvorfor man øker kokepunktet og synker frysepunktet til en væske ved å legge til salt. Å legge til salt på én side av en halvgjennomtrengelig membran gir opphav til et osmotisk trykk.
Partisjonskoeffisienten er forholdet mellom konsentrasjonen av et løst stoff i ett løsemiddel og konsentrasjonen av det samme stoffet i et annet løsemiddel.
En gittermodell for dimerisering av oppløste stoffer i et løsemiddel utledes og brukes til å beskrive hydrofob effekt.
Hva er volatilitet?
Volatilitet er evnen til å bytte mellom to faser. For eksempel når saltvann (blanding av salt og vann) fryser går vannet over i en fast fase (frossen). Vannet er volatilt. Saltet går ikke over i den faste fasen. Saltet er ikke volatilt. Saltet blir værende igjen i den flytende fasen til det felles ut. Det samme gjelder når vann koker. Vann trenger ikke å gå i faseoverganger for å være volatilt. I osmose har vi saltvann på en side av en membran og rent vann på den andre siden. Vannet kan gå mellom den rene og den saltholdige fasen gjennom membranen. Vannet er volatilt. Saltet kan ikke trenge gjennom membranen og er ikke volatilt. Vann er ikke nødvendigvis den volatile fasen. Hvis vi har \(CO_2\) løst i vann ved romtemperatur er \(CO_2\) den volatile fasen. Dette ser vi mer om etterpå. Vi har altså tre eksempler på situasjoner der et stoff er mer volatilt enn det andre: Saltvann i faseovergang, karbondioksid som løses i vann og osmose
Lynutledning damptrykk#
Likevekt er når de kjemiske potentialene for to faser er like
Det kjemiske potentialet til en gass kommer fra kapittel 11 (ligning 11.50)
Det kjemiske potentialet til en væske kommer fra kapittel 15 (ligning 15.17)
Om vi slår disse ligningene sammen kan vi lett utlede damptykket som en funksjon av molfraksjon
Solvatering#
Se for deg at vi har en flytende blanding av to komponenter A og B. B er volatil og A er ikke. Generelt sett for blandinger gjelder det at
der \(p^0_B\) er damptrykket til B.
\(\chi_{AB}\) kalles utvekslingsparameteren og \(\chi_{AB} > 0\) dersom A og B ikke liker hverandre, som f.eks. hvis A er hydrofob og B er hydrofil.
Vi har to forskjellige spesialtilfeller når vi har to stoffer av forskjellig volatilitet. Det ene er at det volatile stoffet er et løsemiddel, altså at det er veldig mye av det. Det gjelder for eksempel i osmose eller når saltvann fryser.
Det andre er at det volatile stoffet er en løsning, altså at det er veldig lite av det. Det gjelder for eksempel når \(CO_2\) løses i vann.
Spesialtilfellene er beskrevet under.
Raoults lov#
Raoults lov gjelder når molfraksjonen til stoffet som kan bevege seg er svært stor, som f.eks. når vi har salt i vann. Den sier at det partielle trykket til en gass er lineært med molfraksjonen til gassen.
Når vi broker Raoults lov impliserer vi at vi har en entropidrevet effekt siden utvekslingsparameteren \(\chi_{AB}\), leddet som har med forskjellene i styrke på intermolekylære bindinger ikke lenger er med i uttrykket.
Man kan også se på det fra omvendt synsvinkel, og si at Raoults lov gjelder når \(\chi_{AB}=0\), altså når A og B molekylene er like glad i hverandre som seg selv. Da er det åpenbart at vi har en entropidrevet effekt, siden forskjellene i bindingsenergi er 0. Raoults lov gjelder dermed for ideelle løsninger.
Utledning
Uttrykket kommer av å ta den generelle formelen for partielltrykk i blandinger, og så sette \(x_B \approx 1\) $\( p*B = p^0_Bx_Be^{\chi*{AB}(1-x_B)^2} \)$
Henrys lov#
Henrys lov gjelder når molfraksjonen til det volatile stoffet er svært stor, f.eks. ved \(CO_2\) løst i vann. Da får vi at \(x_B\rightarrow 0\) og dermed
Vi kan åpenbart ikke tilnærme den gjenstående \(x_B\)-faktoren til 0 fordi da blir hele uttrykket 0.
Osmose#
Osmose er at vann trekker gjennom en membran på grunn av en saltgradient over membranen. Det gjør den fordi multiplisiteten øker. Se figur.
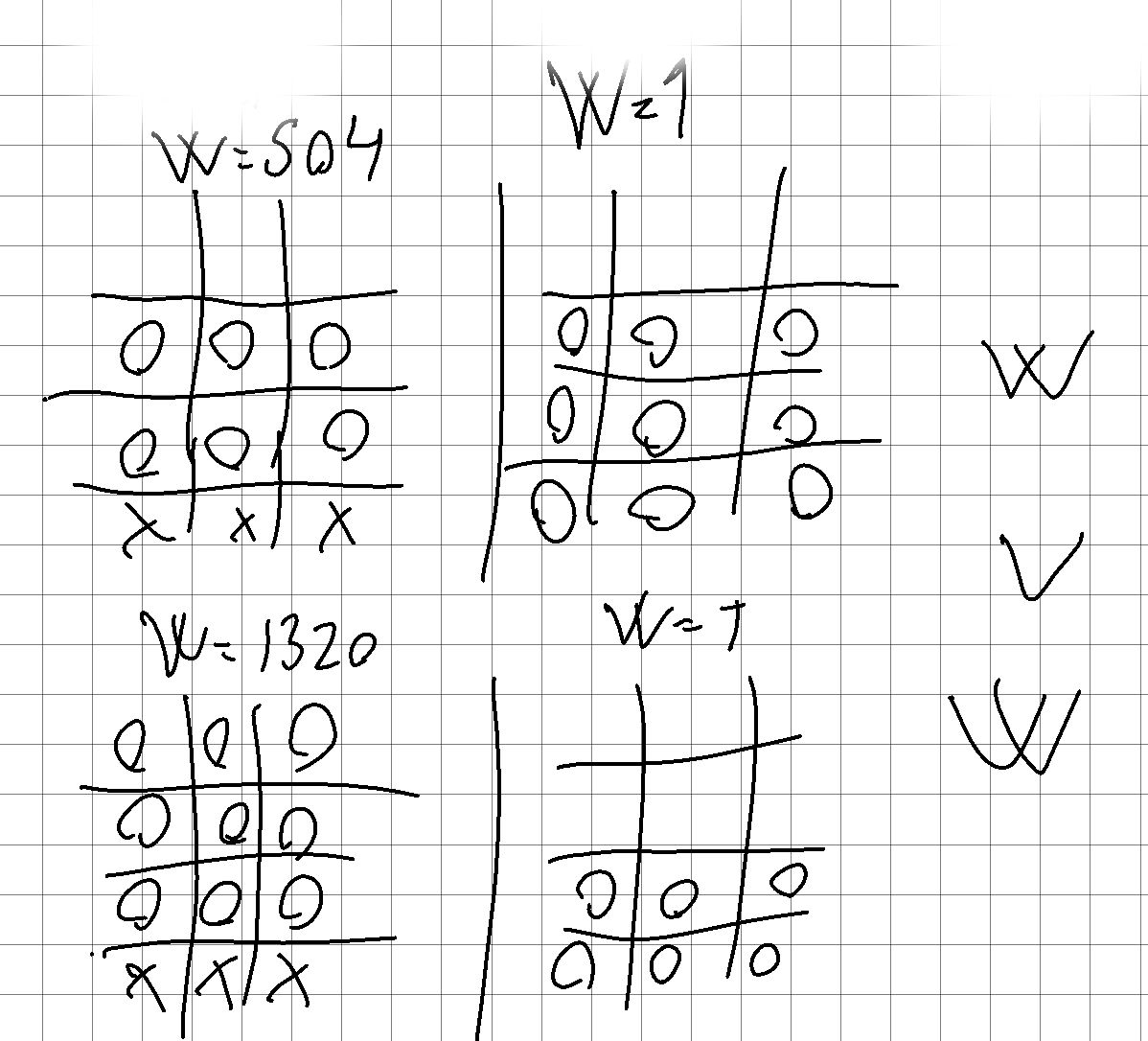
Fig. 1 Multiplisiteten er høyest dersom alt vannet går over til den saltholdige fasen. Dette er drivkraften bak osmose.#
Når vannet reiser over membranen blir det et trykk som motvirker prosessen. Dette kalles osmotisk trykk.
Salt gjør flytende fase mer gunstig#
Salt tilsatt vann gjør den flytende fasen mer gunstig. Det har effektene at salt senker frysepunktet og øker kokepunktet. Det er derfor vi salter veiene, da smelter isen på veien. (Vi salter dessverrre pastavannet av andre grunner). Denne effekten kommer av det samme multiplisitetsprinsippet som osmose.
